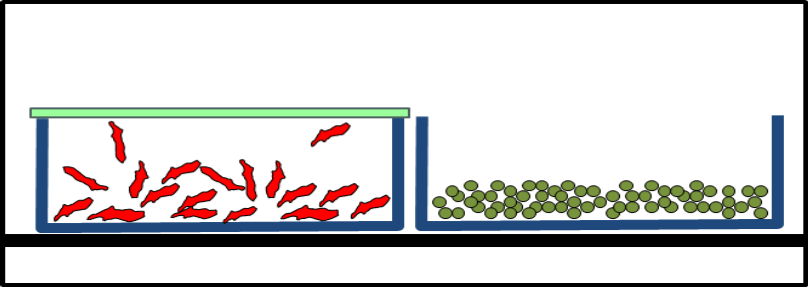
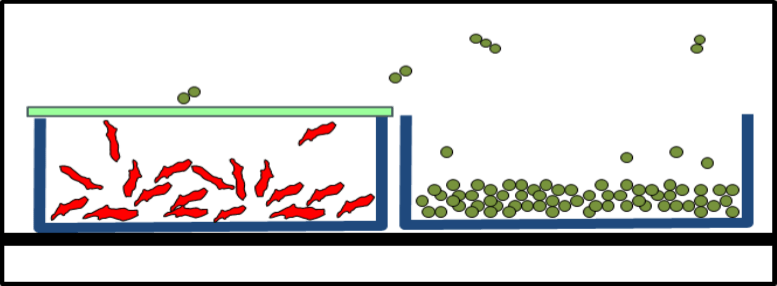
Die Numaferm GmbH verwendet den Teclen® Lyoprotect® Beutel zur Vermeidung von Flyout von Peptiden


Vorstellung der Numaferm GmbH
Die Numaferm GmbH hat sich seit ihrer Gründung 2017 zu einem erstklassigen, zuverlässigen Partner im Bereich der rekombinanten Expression von Peptiden und Proteinen entwickelt.
Im rund 30-köpfigen Expertenteam steht unter anderem das Fachwissen von 15 promovierten Mitarbeitern mit zusammengerechnet über 100 Jahren Expertise in der Prozessentwicklung und Produktion zur Verfügung. Die großzügige Laboranlage ist mit modernster Technologie ausgestattet und bietet somit beste Voraussetzungen für die Entwicklung schneller, kostengünstiger und ressourcenschonender Produktionsprozesse zur Herstellung hochreiner Produkte.
Im Rahmen der von Numaferm entwickelten Technologie-Plattformen, wie NumaswitchTM, werden Zellen des Bakteriums Escherichia coli umprogrammiert, sodass sie das gewünschte Peptid/Protein herstellen. Diese patentgeschützten Verfahren zählen zu den erfolgreichsten am Markt, nicht zuletzt, da die Kosten bei nur einem Zehntel der chemischen Synthese liegen. Mit der NumacutTM TEV Protease hat Numaferm kürzlich zudem ihr erstes eigenes Enzymprodukt kommerzialisiert und somit die bisher intern genutzte Innovations- und Entwicklungsarbeit auch für Kunden/Partner zugänglich gemacht.
Die NumacutTM TEV Protease ist eine hoch aktive, optimierte Variante der Tabacco Etch Virus (TEV) Protease mit einer verbreiterten Substrattoleranz und hoher Stabilität. Zur Gewährleistung einer hohen Lagerstabilität und eines umwelt- und kostenfreundlicheren Versands wird die NumacutTM TEV Protease lyophylisiert und kann im Anschluss bei Raumtemperatur versandt werden.
Ausgangssituation
Im vorliegenden Herstellungsprozess sollten Enzym-Produkte, wie die NumacutTM TEV Protease, als Lyophilisat an Kunden versandt werden. Eine gleichbleibende Produktqualität hatte hierbei höchste Priorität. Die Formulierung sollte flüssig in zum Versand geeignete Gefäße (Vials) eingebracht und anschließend lyophilisiert werden.
Während des Lyophilisationshandlings sollten Flyout und damit einhergehender Produktverlust sowie jegliche Kontamination der Produkte als auch der Umgebung ausgeschlossen werden. Nach der Lyophilisierung sollten die Vials mit dem Stopfen verschlossen werden.
Die Lösung: Lyoprotect® Beutel
Herr Dr. Christian Schwarz kontaktierte die Teclen GmbH, 
um zu erfahren, wie Lyoprotect® Beutel zur Lyophilisierung in Gefäßen (Vials) eingesetzt werden können. Die Anpassbarkeit der Beutelgrößen war ein besonderer Pluspunkt, ebenso der geringe Einfluss der Lyoprotect® Membrane auf die Trocknungsbedingungen im Vergleich zu einem offenen Vial und selbstverständlich die hervorragenden Barriere-Eigenschaften der Lyoprotect® Beutel.
Die in einer Lagerbox befüllten Lyo-Gefäße werden in den Lyoprotect® Beutel geschoben – die Beutel befinden sich dabei bereits in dem Gefriertrockner – und anschließend mit dem Klemmsystem verschlossen und gesichert. Nach erfolgter Gefriertrocknung können die Vials mit Lyo-Stopfen an Ort und Stelle mit einer Hilfsplatte sicher verschlossen werden.
Die Numaferm GmbH verwendet nun seit längerem Lyoprotect® Beutel erfolgreich in der Lyophilisation flüssiger Peptidformulierungen im präparativen Maßstab.

CEO bei Numaferm
„Die Verwendung der passenden Lyoprotect® Beutel verbessert sowohl das Produkthandling als auch die Mitarbeitersicherheit gegenüber Produktstäuben. Die verschiedenen Lyoprotect® Beutelgrößen schaffen hierbei eine größtmögliche Flexibilität bei unterschiedlichen Chargengrößen und Abfüllungen, was sowohl in unserem Dienstleistungs- als auch Produktbusiness gleichermaßen wichtig ist.“
NumacutTM ist eine Marke der Numaferm GmbH.
Zum Produkt der Numaferm GmbH, NumacutTM TEV Protease
Kontaktieren Sie uns gerne bei Fragen oder für Ihr persönliches Angebot!






 Vorstellung der Lactosan GmbH & Co KG
Vorstellung der Lactosan GmbH & Co KG